黔驴技穷?解决难治性狼疮肾炎或许应另辟蹊径……
分享难治性LN诊疗经过和思路。
2011年4月,出现手关节肿痛,无其他系统症状,于外院诊断为SLE,予以泼尼松、羟氯喹(HCQ)联合吗替麦考酚酯(MMF)治疗,病情基本稳定;
2017年3月,尿蛋白升高,考虑LN。原治疗方案调整剂量至泼尼松10mg QD HCQ 0.2g BID MMF 0.75g BID;
2017年7月,意外妊娠,将原治疗方案中MMF换为他克莫司(TAC)3mg QD,泼尼松和HCQ用量不变;
2017年9月,患者周身浮肿。激素(泼尼松)用量增至17.5 mg QD,但浮肿变化不大,改善不明显;
2017年12月第一次住院,尿蛋白定量13.58 g/d;查生化指标:白蛋白(ALB)14.9 g/L,尿素13.48 mmol/L,总胆固醇 2.43 mmol/L;炎症指标:红细胞沉降率(ESR)47 mm/h,C反应蛋白(CRP)7.4 mg/L;免疫指标:抗核抗体(ANA)颗粒1:3200,anti-ds-DNA 1:320,抗U1-RNP阳性,抗Sm阳性,抗核小体抗体阳性,抗组蛋白抗体阳性;彩超示双肾弥漫性增大、双侧胸腔、腹腔积液。诊为SLE LN。后胎心消失,引产。治疗:停用TAC,予以甲泼尼龙琥珀酸钠 80 mg*8天,泼尼松70mg QD HCQ 0.2g BID MMF 1.0g BID 贝那普利10mg BID;
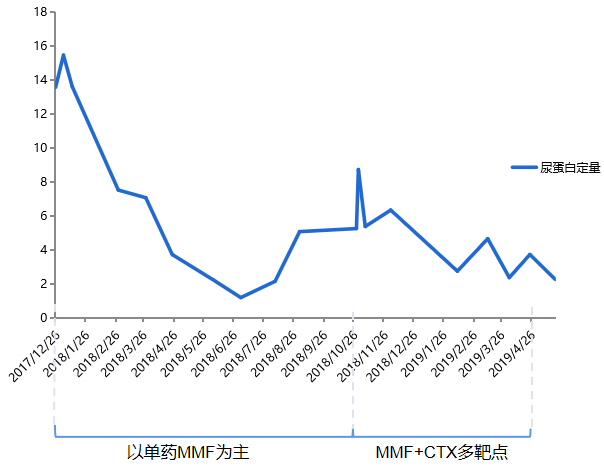
2018年7月,复查24h尿蛋白1.18g/d,予以泼尼松5mg QD HCQ 0.2g BID MMF 0.5g BID 贝那普利10mg BID继续治疗;同年9月复查,24h尿蛋白增至5.07 g/d,MMF剂量增至0.75g BID,并加用来氟米特(LEF)10 mg QD;2018年11月复查尿蛋白5.37 g/d,提示病情仍然活动,予以激素联合免疫多靶点治疗:甲泼尼龙琥珀酸钠 80 mg*5天→泼尼松30mg QD,MMF 0.5g BID 环磷酰胺(CTX)100 mg QOD HCQ 0.2g BID 贝那普利10mg BID;
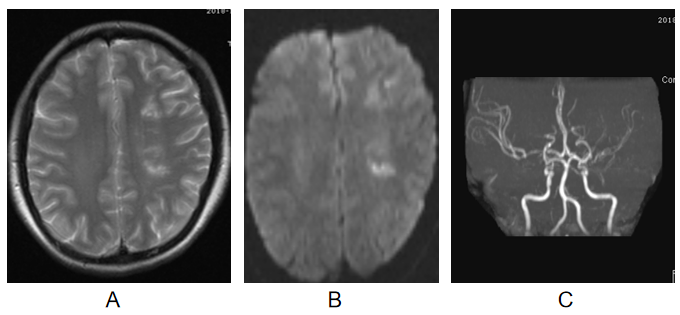
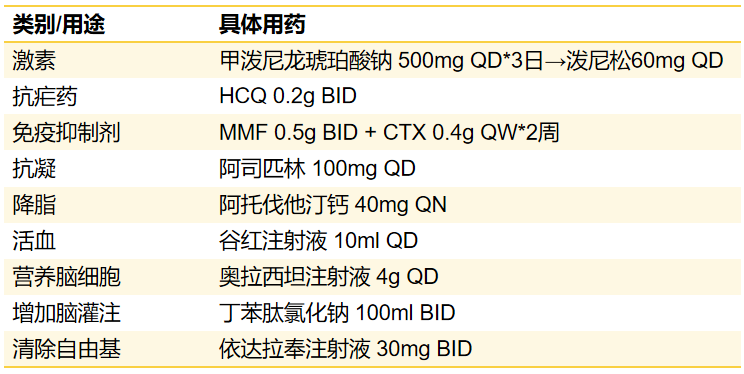
2018年11月,患者右手第3-5指间断出现麻木症状,12月晨起后自觉言语不利、语速慢。查体示血压(BP)141/80mmHg,双手可见散在红斑皮疹,神经系统查体无异常;辅助检查示,尿蛋白定量 6.34 g/d、甘油三酯(TG)5.58 mmol/L、低密度脂蛋白-c(LCL-c) 3.23 mmol/L,脂蛋白(Lpa) 449 g/L;炎症指标ESR 35 mm/h,CRP 9.40 mg/L。头颅影像学检查结果示,左侧额顶叶梗死、双侧颈内动脉及大脑中动脉多发狭窄(图1),考虑神经精神性狼疮(NPSLE)。诊断为SLE、LN、NPSLE、急性脑梗死、双侧大脑中动脉狭窄,病情评估为重度活动(SLEDAI评分22分)。治疗方案:激素联合抗疟药、免疫抑制剂,并进行抗凝、降脂、活血、营养脑细胞、增加脑灌注、清除自由基等治疗(具体用药方案见表1)。
2018年12月至2019年5月20日期间,调整用药方案为MMF 0.5g BID CTX(0.4g QW*2→0.6g QW*8,累计5.6g) 阿司匹林 100 mg QD 阿托伐他汀钙 20 mg QN ,泼尼松规律减量至10mg QD和15mg QD交替应用,尿蛋白最低2.25g。
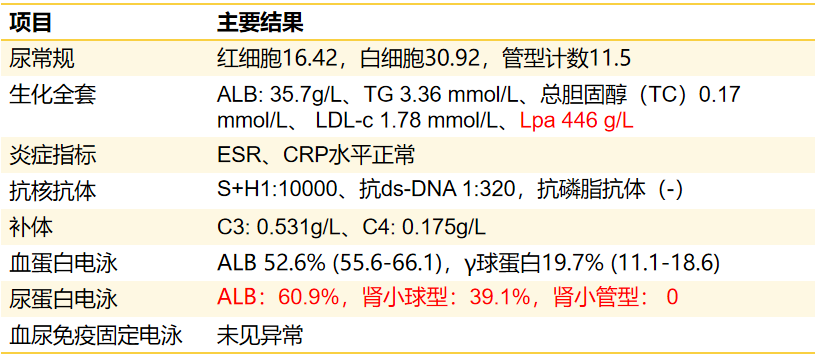
2019年5月26日,为行肾穿刺活检住院,进行辅助检查(结果见表2)。肾穿刺病理符合Ⅳ-A Ⅴ型LN表现,2019年6月3日出现左下肢无力,颅脑影像学检查(结果见图3),考虑多发脑梗塞。
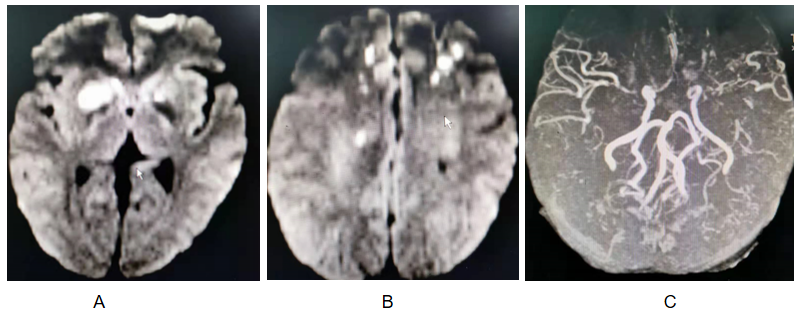
2019年6月4日转入神经内科。经颅多普勒超声检查(TCD)示,1、右大脑中动脉深度流速明显增快,伴涡流杂音;左大脑中动脉流速快,伴涡流,鸥鸣样杂音;左大脑前动脉流速快,伴涡流,鸥鸣样杂音;2、右大脑后动脉:双椎动脉、基底动脉流速快,频谱紊乱,伴杂音;左大脑后动脉流速快,频谱紊乱,声粗糙。治疗:加用TAC 1mg BID,患者左下肢肌力好转、右肾血肿,停抗凝及活血药物;后患者出现左下肢麻木,加用阿司匹林 75mg QD、丁苯酞和奥拉西坦,复查头颅MRA、DWI,无新发脑梗,脑血流灌注情况较前改善(图4)。2019年6月24出院。

2019年6月25日至2019年10月11日:泼尼松 15mg QOD HCQ 0.2g BID MMF 0.5g BID TAC 1mg BID,10月14日查尿蛋白1.78g/d;TCD流速180;
2019年10月12日至2020年1月15日:泼尼松 10mg QOD HCQ 0.2g BID MMF 0.5g BID TAC 1mg BID,1月15日查尿蛋白1.51 g/d,5月13日复查尿蛋白2.02 g/d;
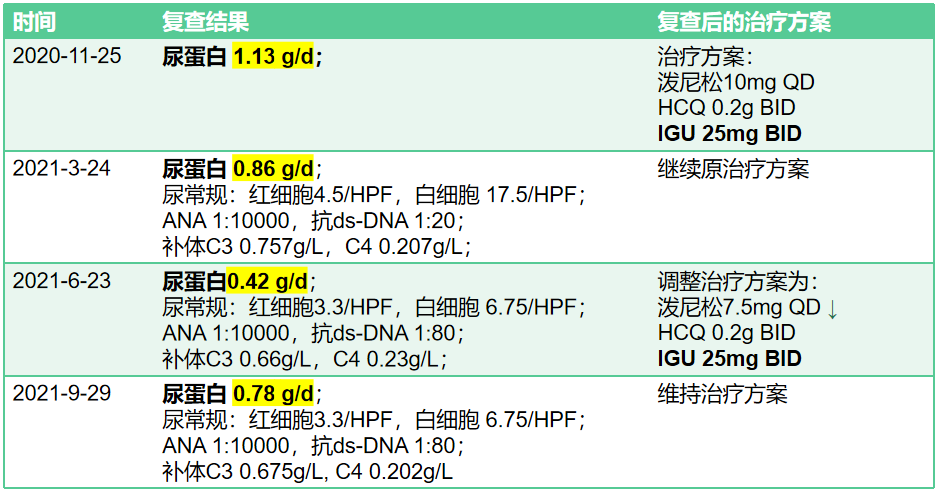
2020年5月14日至2020年8月19日:调整治疗为泼尼松15mg QD HCQ 0.2g BID LEF 20mg QD 雷公藤20mg TID,8月19日查尿蛋白1.67 g/d,11月25日复查尿蛋白1.13 g/d,且患者出现闭经。故调整治疗方案为:泼尼松10mg QD HCQ 0.2g BID IGU 25mg BID,IGU治疗期间随访数据见表3。
案例小结
2011年被诊断为SLE后,应用激素 HCQ MMF方案治疗约6年,病情基本稳定;
2017年3月出现尿蛋白升高,考虑LN。应用激素、HCQ联合免疫抑制剂(以MMF为主,包括CTX、TAC等)治疗近2年,病情仍未能有效缓解;
并发NPSLE后,应用大剂量激素冲击后,序贯激素联合CTX、MMF治疗,病情得到部分缓解,期间行肾穿刺,病理诊断符合Ⅳ-A Ⅴ型狼疮肾炎;
肾穿后病情再次反复,出现多发性脑梗塞,加用TAC控制LN,应用抗血小板、改善脑血流灌注等治疗后病情部分缓解;继续以激素、HCQ联合免疫抑制剂治疗7月余,病情相对平稳,但尿蛋白持续存在(>1g/d,最高时超过2g/d);
2020年11月出现闭经,停用原来的免疫抑制剂,换用激素、HCQ联合IGU的方案,尿蛋白降至1g/24h以下,接近完全缓解,继续随访至今,病情稳定。

河北医科大学第三医院
风湿免疫科副主任,医学博士,副教授,硕士研究生导师
河北省医学会风湿免疫学会委员
河北省药学会风湿免疫药学专业委员会委员
河北省医师学会委员
河北省医疗事故鉴定专家库成员
热门药品