PD-1联合CTLA-4,免疫细胞先集合再突破,癌细胞无处遁形
前列腺癌是男性常见癌症之一,2018年全球新诊断出近128万病例。与早期前列腺癌不同,去势抵抗性前列腺癌(CRPC)患者即使接受内分泌治疗使体内睾酮量降低,但癌细胞仍可以继续增长。所幸的是,在接受激素治疗和化疗失败后的一些患者,对免疫治疗产生了反应。
肿瘤免疫治疗最常见的方式,就是用抗体阻断免疫检查点蛋白的结合,从而激活免疫细胞对癌细胞的杀伤能力。但这一方法必须建立在肿瘤组织当中存在免疫细胞的基础上,巧妇难为无米之炊,转移去势抵抗性前列腺癌前列腺癌(mCRPC)就是病灶中免疫细胞数量极少的那一类,所以免疫治疗很难起效。
2019年初,美国德州大学安德森癌症研究中心就发表了一项临床试验的早期结果:一些转移性前列腺癌患者对免疫检查点抑制剂的组合有反应!
研究将患者分为两组,A组为激素治疗失败的去势抵抗患者,B组为激素治疗和化疗均失败的去势抵抗患者。两组患者均同时接受免疫药物PD-1抑制剂和CTLA-4抑制剂治疗,结果显示:

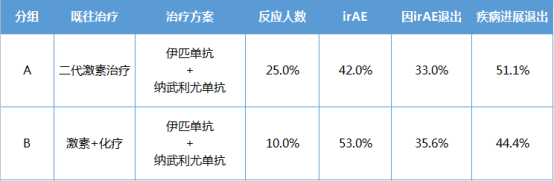
这是在前列腺癌中使用两种免疫检查点疗法的首次联合试验。这些结果支持了免疫检查点抑制剂可以在这些患者的治疗中发挥重要作用的想法,并为在更大的临床试验中测试该策略提供了基础。
——首席研究员Padmanee Sharma教授
在此前的I期试验中,没有患者对纳武利尤单抗(PD-1抑制剂)产生反应,因为它需要肿瘤病灶中存在免疫细胞才能够攻击肿瘤。而另一项试验中,伊匹单抗(CTLA-4抑制剂)和抗激素药物Lupron联用治疗前列腺癌,治疗前后的肿瘤样品分析结果显示,伊匹单抗能够诱导T细胞渗透进入肿瘤组织内部,进而引起肿瘤内的免疫反应。
2020年4月,由美国大学牵头的一项II期临床试验结果在《科学转化医学》杂志上发布。某些患有转移去势抵抗性前列腺癌(mCRPC)的患者在接受了伊匹单抗(CTLA-4抑制剂)治疗后,其肿瘤中的活性T细胞数量增加,并且患者生存期得到延长。
我们的结果表明,尽管前列腺癌的肿瘤突变负荷(TMB)很低,但免疫检查点抑制剂(ICI)仍可促进T细胞对肿瘤新抗原的反应。
我们在受益最大的一部分患者中发现了特定的标志物:如T细胞密度和干扰素-γ信号传导,这些标志物可能有助于提高我们筛选接受ICI治疗的患者的能力。
——泌尿生殖医学肿瘤学助理教授
Sumit Subudhi博士
此项试验纳入30例转移去势抵抗性前列腺癌(mCRPC)患者,他们中有29位至少接受过一剂伊匹单抗(CTLA-4抑制剂)治疗并被纳入分析。经统计,所有患者的中位无进展生存期(mPFS)为3个月,中位总生存期(mOS)为24.3个月。其中有28%(8例)的患者最高经历了3级irAE。
进一步地,将“PFS>6个月且OS>24个月”的患者定义为“有利”组(共9位),将“PFS<6个月且OS<24个月”的患者定义为“不利”组(共10位),分析发现:“有利”组的患者肿瘤中有更多数量的T细胞,以及更高水平的干扰素γ(IFN-γ)。此外,从“有利”组患者肿瘤中分离出的T细胞更容易识别和杀伤产生新抗原的癌细胞。
我们感到鼓舞的是,具有低肿瘤突变负荷(TMB)的mCRPC患者,肿瘤中表达的新抗原会引起T细胞反应,从而导致良好的临床结果。
我们的研究结果表明,利用CTLA-4抑制剂治疗mCRPC的方法值得进一步研究,以开发可改善此类患者生存率的治疗策略。
——Sharma博士
近日,一项名为CheckMate 650的研究结果发表在《癌症》杂志上。研究纳入90名转移去势抵抗性前列腺癌(mCRPC)患者,每三周接受一次PD-1抑制剂(纳武利尤单抗)与CTLA-4抑制剂(伊匹单抗)治疗,结果显示:


这项评估旨在探索双免疫联合治疗mCRPC患者的更优给药方案以改善免疫治疗的安全性。研究人员假设CTLA-4抑制剂(伊匹单抗)与抗PD-1抑制剂(纳武利尤单抗)联合使用,可以有效地将T细胞引入肿瘤病灶中,并克服所产生的免疫抑制反应。随后的结果表明,有些患者因治疗而受益明显,但还有部分患者因治疗产生的严重irAE而不得不中断免疫治疗,因此,研究者们需要通过修改给药方案来提高双免疫疗法的安全性。
从历史上看,前列腺癌对ICI疗法具有很强的抵抗力,因为它在几乎没有肿瘤浸润的T细胞。此项研究结果表明,增加T细胞浸润,然后再阻断免疫检查点蛋白的结合,这种联合方法可能是治疗这些患者的有用策略。展望未来,我们计划进一步优化计划和剂量以改善安全性。
——首席研究员Padmanee Sharma博士
此外,研究小组还鉴定了与患者临床结果相关的潜在生物标志物,他们发现,PD-1单抗 CTLA-4单抗的组合免疫疗法对肿瘤突变负荷(TMB)较高的患者可能更有效。
我们希望,肿瘤的免疫治疗不仅需要“从有药到无药”,也需要“从有效到安全”。CheckMate 650研究迄今为止产生的数据令人鼓舞,但他们仍在安全性方面需要寻找毒性更小的联合用药策略。
热门药品