泰吉华(阿伐替尼)说明书(疗效_价格_副作用)
关于“泰吉华(阿伐替尼)说明书(疗效_价格_副作用)”的相关内容,相信很多病友都想知道,为了方便大家了解,觅健小编搜集整理了有关“泰吉华(阿伐替尼)说明书”的一些资料分享给大家,希望能帮助到大家,供参考。
阿伐替尼(泰吉华)说明书
请仔细阅读说明书并在医师指导下使用

【药品名称】
通用名称:阿伐替尼片
商品名称:泰吉华,AYVAKIT
英文名称:Avapritinib
汉语拼音:Afatini Pian
【成份】
阿伐替尼主要活性成份为阿伐替尼
化学名称:(S)-1-(4-氟苯基)-1-(2-(4-(6-(1-甲基-1H-吡唑-4-基)吡咯[2,1-f][1,2,4]三嗪-4-基)哌嗪基)嘧啶-5-基)-1-乙胺
【性状】
本品为白色圆形(100mg规格)或椭圆形(200mg和300mg规格)薄顺衣片,除去包衣后显白色、类白色或黄色。片剂一面印有“BLU”字样、另一面印有:100(100mg规格)成200”(200mg规格)或*300”(300mg规格)字样。
【适应症】
本品适用于治疗携带血小板衍生生长因子受体a(PDGFRA)外显子18突变(包括PDGFRA D842V突变)的不可切除或转移性胃肠道间质瘤(GIST)成人患者。
【规格】
(1) 100mg (2)200mg (3)300mg
【用法用量】
本品应在有肿瘤治疗经验的医生指导下使用。
患者选择
使用本品治疗前必须明确有经充分验证的检测方法检测到PDGFRA外显子18突变。
推荐剂量
本品推荐口服剂量为300 mg,每日一次,至少在餐前1小时和餐后2小时空腹给药。持续治疗,直至出现疾病进展或不可接受的毒性。请勿在距离下次计划给药时间不足8小时前补服漏服剂量。
如果服用本品后发生呕吐,请勿补服,只需按预定时间继续服用下一剂。
避免阿伐替尼与强效或中效CYP3A抑制剂合用。如果无法避免与中效CYP3A抑制剂合用,则将阿伐替尼的起始剂量从300mg每日一次降低至100mg每日一次(见【药代动力学】)。
针对不良反应的剂量调整
表1 用于控制不良反应时推荐的降低剂量
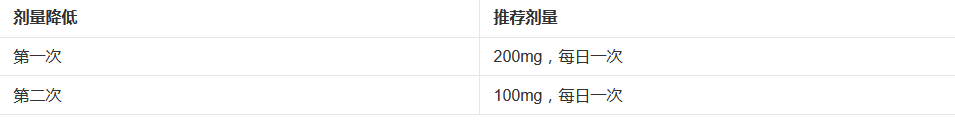
无法耐受100mg每日一次剂量的患者,永久停用阿伐替尼。
表2 阿伐替尼的剂量调整原则
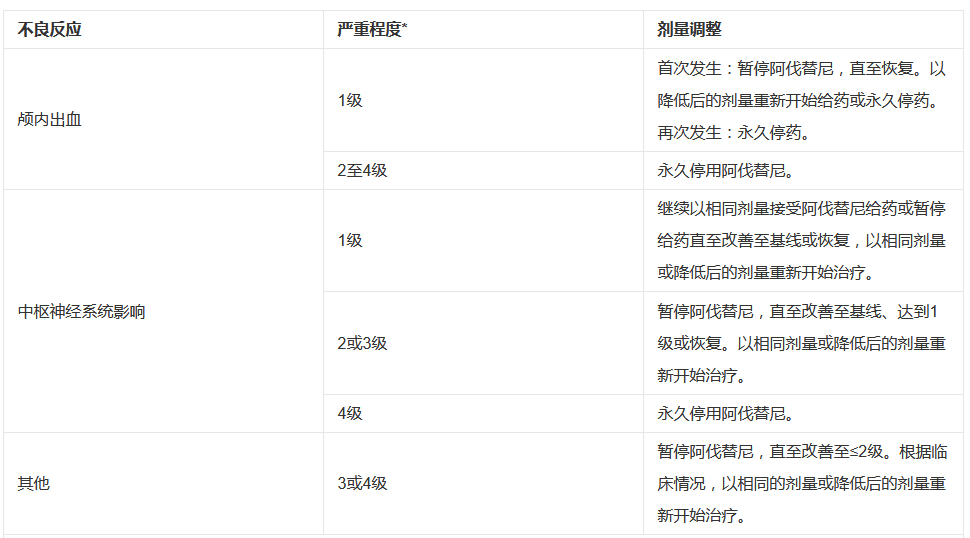
特殊人群
儿童用药
18岁以下儿童和青少年患者慎用。
老年用药
建议老年患者应在医生指导下慎用阿伐替尼,无需调整起始剂量。
肝损害患者
对于轻度(总胆红素≤正常值上限[ULN]且天门冬氨酸氨基转移酶(AST)>ULN,或总胆红素>1-1.5倍ULN且AST值不限)或中度(总胆红素>1.5-3倍ULN,AST值不限)肝损害患者,不建议调整剂量。尚未确定本品在重度肝损害患者中的安全性和有效性,重度肝损害患者慎用。
肾损害患者
对于轻度和中度肾损害患者[Cockcroft-Gault公式估算的肌酐清除率(CLcr)为30-89mL/min] ,不建议调整剂量。尚未确定本品在重度肾损害(CLcr为15-29mL/min)或终末期肾病(CLcr<15mL/min)患者中的安全性和有效性,重度肾损害患者慎用。 [
孕妇及哺乳期妇女用药
妊娠
目前尚无阿伐替尼对孕妇影响的临床研究。基于动物试验结果及本品的作用机制,孕妇服用本品后,可能会对胎儿造成伤害。妊娠大鼠在器官形成期经口给予阿伐替尼,暴露量约为人体300 mg剂量下暴露量的2.7倍时,出现致畸性和胚胎毒性。妊娠期间禁止使用本品。
哺乳
目前尚不明确阿伐替尼是否经人乳汁排泄。由于大多数药物经乳汁排泄,故不能排除本品对哺乳婴儿的风险。本品治疗期间,必须停止哺乳。
【不良反应】
安全性特征总结
阿伐替尼的安全性特征总结基于接受阿伐替尼起始剂量为300mg或400mg的550例GIST患者的汇总数据。
接受阿伐替尼治疗期间,最常报告的不良反应包括恶心(45%)、疲乏(40%)、贫血(39%)、眶周水肿(33%)、面部水肿(27%)、高胆红素血症(28%)、腹泻(26%)、呕吐(24%)、外周水肿(23%)、流泪增加(22%)、食欲下降(21%)和记忆受损(20%)。23%的患者发生严重不良反应,最常见的严重不良反应为贫血(6%)和胸腔积液(1%)。
9.6%的患者发生导致永久停药的不良反应,最常见的不良反应为疲乏、脑病和颅内出血(均<1%)。48.7%的患者发生导致剂量下调的不良反应,包括贫血(8.7%)、疲乏(6.5%)、中性粒细胞计数降低(4.9%)、血胆红素升高(4.7%)、记忆受损(3.8%)、认知障碍(3.1%)、眶周水肿(2.4%)、恶心(2.2%)和面部水肿(2.2%)。
特定不良反应的描述
颅内出血
550例以300mg或400mg每日一次起始剂量接受阿伐替尼治疗的GIST患者中,9例(1.6%)发生颅内出血(例如硬膜下血肿、颅内出血、大脑出血和大脑血肿)(见【注意事项】)。其中,6例(1.1%)发生≥3级颅内出血事件,1例发生2级颅内出血事件,未发生导致死亡的颅内出血事件。8例患者因颅内出血进行了阿伐替尼用药剂量调整。
颅内出血事件(所有级别)发生在开始接受阿伐替尼治疗后8周至84周范围内,中位至事件发生时间为22周。≥2级颅内出血的中位至改善和恢复时间为25周。
认知影响
550例以300mg或400mg每日一次起始剂量接受阿伐替尼治疗的GIST患者中,182例(33%)发生认知影响(见【注意事项】)。在发生该事件(任何级别)的患者中,中位至事件发生时间为8周。
多数认知影响为1级(22%),11%的患者发生≥2级认知影响(其中2级、3级分别为9%和2%,无4级及以上事件)。在发生≥2级(影响日常生活活动)认知影响的患者中,中位至改善时间为15周。
20%的患者出现记忆受损,其中3级事件占比<1%。12%的患者出现认知障碍,其中3级事件占比<1%。5%的患者出现意识模糊状态,其中3级事件占比<1%。<1%的患者出现脑病,其中3级事件占比<1%。1.3%的患者报告了严重的认知影响。
总体而言,13.1%的患者因认知影响进行了阿伐替尼用药剂量调整,1.3%的患者因认知影响永久停用阿伐替尼。
以300mg或400mg起始剂量接受阿伐替尼每日一次治疗的≥65岁患者中,37%的患者发生了认知影响。
液体潴留
550例以300mg或400mg每日一次起始剂量接受阿伐替尼治疗的GIST患者中,70.2%的患者发生了水肿,包括局部水肿(面部、眶周、外周水肿和胸腔积液)和全身水肿。其中,4.7%的患者发生了≥3级水肿,10.4%的患者因水肿进行了阿伐替尼用药剂量调整。>1%的患者发生的导致剂量调整的水肿反应为眶周水肿(3.6%)、面部水肿(3.5%)和外周水肿(2.2%)。
【药物相互作用】
强效和中效CYP3A抑制剂
与强效或中效CYP3A抑制剂联用可增加阿伐替尼的血浆浓度,这可能会增加不良反应的发生率和严重程度。避免与强效或中效CYP3A抑制剂联用。
如果无法避免与中效CYP3A抑制剂联用,则应降低剂量。
强效和中效CYP3A诱导剂
与强效或中效CYP3A诱导剂联用可降低阿伐替尼的血浆浓度,可能会降低疗效。避免与强效或中效CYP3A诱导剂联用。
对P-糖蛋白(P-gp)和乳腺癌耐药蛋白(BCRP)有抑制作用,但不是P-gp和BCRP的底物。患者应避免或慎重合并使用P-gp或BCRP底物,如需合用应密切监测不良反应。
与质子泵抑制剂联用时,未发现药代动力学差异具有临床意义。
【禁忌】
对任何成分过敏者禁用。
【临床试验】
胃肠道间质瘤全球研究
NAVIGATOR是一项全球多中心、单臂、开放标签临床试验,入组患者为确诊的GIST患者,ECOG体能状态(PS)评分为0-2。患者口服阿伐替尼300mg或400mg每天一次直至疾病进展或出现不可接受的毒性。试验最初入组患者的起始剂量为400mg,随后由于毒性降低至推荐剂量300mg。由于与接受400mg每日一次治疗的患者相比,接受300mg每日一次治疗的患者的总体缓解率(ORR)无明显差异,因此将这些患者合并进行疗效评价。主要疗效终点指标是采用改良的RECIST v1.1标准通过独立影像学审查进行疾病评估的ORR,其中淋巴结和骨转移灶不作为靶病灶,原发肿瘤内的新生肿瘤结节需≥2 cm,且明确为活动性病灶,必须至少连续2次影像学检查确定病灶进行性增大才视为疾病进展。另一项疗效评估终点指标为缓解持续时间(DOR)。
携带PDGFRA外显子18突变的GIST患者
对于携带PDGFRA外显子18突变的不可切除或转移性GIST患者,在当地或中心实验室采用基于PCR或NGS测序方法进行确定。疗效评估基于43例患者,其中38例患者为PDGFRA D842V突变。43例患者的中位随访持续时间为10.6个月(范围:0.3-24.9个月)。
研究人群的中位年龄为64岁(范围:29-90岁),67%为男性,67%为高加索人,93%的ECOG PS评分为0-1,98%有转移性疾病,53%的最大靶病灶>5 cm,86%为既往接受过手术切除。既往接受激酶抑制剂的中位治疗数量为1(范围:0-5)。
截至2018年11月16日,在NAVIGATOR中携带PDGFRA外显子18突变的GIST患者(包括PDGFRA D842V突变患者)的疗效结果总结如下表:

缩写:CI=置信区间;NR=未达到
表示持续缓解中。
1该人群中非D842V的外显子18突变为:缺失突变D842_H845(n=3);D842Y(n=1);缺失突变D842_H845合并插入突变V(n=1)。
*11例持续缓解患者的随访时间(从出现缓解开始计算)<6个月。
【药理毒理】
药理作用
阿伐替尼是一种酪氨酸激酶抑制剂,靶向PDGFRA和PDGFRA D842突变体以及KIT外显子11、11/17和17等多个突变体,半数抑制浓度(IC50s)小于25nM。PDGFRA和KIT的某些突变可导致这些受体出现自磷酸化和结构性激活,从而促进肿瘤细胞增殖。阿伐替尼的其他潜在靶点包括野生型KIT、PDGFRB和CSFR1。
体外细胞试验中,阿伐替尼可抑制与已上市的激酶抑制剂相关的KIT D816V和PDGFRA D842V耐药突变体的自磷酸化,IC50分别为4nM和30nM。在植入来源于GIST患者的伊马替尼耐药并携带活化KIT外显子11/17突变的异种移植瘤小鼠模型中,阿伐替尼也表现出抗肿瘤活性。
毒理研究
遗传毒性
体外细菌回复突变试验(Ames试验)显示,未见阿伐替尼致突变性。体外人外周血淋巴细胞染色体畸变试验显示,阿伐替尼可致染色体断裂。大鼠体内骨髓微核试验结果为阴性。
生殖毒性
阿伐替尼可能损伤人的生育力。雌性大鼠连续3个月给予阿伐替尼≥5mg/kg/天(以AUC计,约为人用剂量300mg时暴露量的1.3倍),导致黄体囊性变性。雄性犬连续3个月给予阿伐替尼≥7.5mg/kg/天(以AUC计,约为人用剂量300mg时暴露量的0.4倍),导致精子生成减少。
妊娠大鼠于器官发生期经口给予阿伐替尼≥10mg/kg/天(以AUC计,约为人用剂量300mg时暴露量的2.7倍)时,导致胎仔体重下降、着床后丢失、内脏(脑积水、间隔缺损和肺动脉干狭窄)和骨骼(胸骨)畸形增加。
致癌性
尚未开展阿伐替尼的致癌性研究。
其他毒性
重复给药毒性试验中,大鼠和犬连续3个月给予阿伐替尼≥ 30mg/kg/天剂量(以AUC计,约为人用剂量300mg时暴露量的1.5倍),引起震颤;犬给予阿伐替尼≥7.5mg/kg/天剂量(以AUC计,约为人用剂量300mg时暴露量的0.4倍),出现脑和脊髓出血以及脑脉络丛水肿。
【药代动力学】
阿伐替尼在30mg至400mg每日一次剂量范围内(推荐剂量的0.1至1.33倍),Cmax和AUC随剂量成比例增加。
给予推荐剂量300mg每日一次时,平均(CV%)稳态Cmax为813 ng/mL(52%),平均(CV%)稳态浓度-时间曲线下面积(AUC0-24h)为15400 h•ng/mL(48%)。每日一次给予,第15天时达到了稳态浓度,重复给药后的平均蓄积比为3.1-4.6。
吸收
单次给予阿伐替尼30mg-400mg(推荐剂量的0.1-1.33倍)后,中位达峰时间(Tmax)为给药后2.0-4.1小时。
食物影响
阿伐替尼伴高热量、高脂肪餐(约909卡路里、58 g碳水化合物、56 g脂肪和43 g蛋白质)服用时,与空腹状态给药相比,阿伐替尼的Cmax和AUC0-INF分别增加59%和29%。
分布
阿伐替尼的平均表观分布容积为1200 L(43%)。在体外研究中,阿伐替尼的蛋白结合率为98.8%,且不具有浓度依赖性。全血-血浆比为0.95。
消除
单次给予阿伐替尼30mg至400mg(推荐剂量的0.1至1.33倍)后,本品的平均血浆消除半衰期为32-57 h。阿伐替尼的稳态平均表观口服清除率为19.5 L/h(48%)。
代谢
在体外,阿伐替尼主要经CYP3A4代谢,少量经CYP2C9代谢。健康受试者单次口服约310 mg放射性标记的阿伐替尼后,主要循环化合物为原型阿伐替尼(49%)及其代谢产物M690(羟基葡萄糖醛酸,35%)和 M499(氧化脱氨基,14%)。患者服用300mg每日一次后,M499的稳态AUC约为阿伐替尼 AUC的80%。在推荐剂量下,M499对疗效产生影响的可能性不大。
排泄
健康受试者单次口服约310mg放射性标记的阿伐替尼后,在粪便中回收到70%的放射性剂量(11%为原型药物),在尿液中回收到18%的放射性剂量(0.23%为原型药物)。
【注意事项】
出血
在不可切除或转移性GIST患者中,阿伐替尼与出血事件发生率增加相关,包括严重和重度事件,例如胃肠出血、肝出血、肿瘤出血和颅内出血。胃肠出血事件是接受阿伐替尼治疗期间最常报告的出血事件(见【不良反应】)。
出血事件的常规监测应包括体格检查,还应每2~3周监测血细胞计数和凝血参数,尤其是存在易出血体质、以及接受抗凝剂(例如华法林和苯丙香豆素)或其他增加出血风险的合并用药治疗的患者。
对于已发现出血的患者,应报告医生出血部位和严重程度,并在出血恢复前每周监测血细胞计数和凝血参数,≥3级出血应立即停药并就医。
颅内出血
接受阿伐替尼治疗的不可切除或转移性GIST患者曾报告颅内出血严重不良反应(见【不良反应】)。
在开始接受阿伐替尼治疗前,携带风险因素(例如重度血小板减少症、高血压、基线存在脑转移病灶)的患者和颅内出血风险增加(例如存在动脉瘤或过去一年内有颅内出血史、有脑血管意外或短暂性脑缺血发作史)的患者应由医生根据患者接受治疗的获益风险,评估是否用药。
阿伐替尼治疗期间出现临床相关的神经系统体征和症状(例如重度头痛、视力问题、嗜睡或局部无力)的患者应立即停药并报告医生。医生可根据临床表现和严重程度酌情通过磁共振成像法(MRI)或计算机断层扫描法(CT)等措施对患者进行颅内出血排查。
明确用药后出现颅内出血的患者,应暂停直至出血恢复,由医生评估以降低的剂量重新开始给药或永久停药(见【用法用量】)。
尚无脑部转移患者使用阿伐替尼的临床试验经验。
认知影响
接受阿伐替尼治疗的不可切除或转移性GIST患者可能发生认知影响(见【不良反应】)。包括记忆受损、认知障碍、意识模糊状态和脑病。认知影响的发生机制尚不明确。
用药期间应常规监测患者的认知功能,如果患者出现新发认知相关症状(健忘或健忘增加、意识模糊或认知功能障碍)或认知症状加重,应立即向医生报告。
患者接受阿伐替尼治疗期间如出现治疗相关认知影响,医患应按照【用法用量】所列情况进行剂量调整。在临床试验中,与未进行剂量调整的患者相比,进行减量或中断给药的患者的认知影响改善。
液体潴留
接受阿伐替尼治疗的不可切除或转移性GIST患者曾报告液体潴留(见【不良反应】)。
服药期间出现水肿的患者,应至少每周称量体重,并评估呼吸困难症状是否加重。如果水肿加重、短期内体重增加明显(一周体重增加1kg),或出现呼吸困难加重,应报告医生并采取妥当的支持性护理和治疗措施,例如考虑暂停给药并接受利尿剂治疗。
QT间期延长
在临床试验中,接受阿伐替尼治疗的不可切除或转移性GIST患者曾观察到QT间期延长。QT间期延长可能导致室性心律失常(包括尖端扭转型室性心动过速)风险增加。
已知存在QT间期延长或面临QT间期延长风险(例如,由于合并用药、既存心脏疾病和/或电解质紊乱)的患者应慎用阿伐替尼。应避免合并使用中效或强效CYP3A4抑制剂,因为可能导致发生不良反应的风险增加,包括QT间期延长和相关心律不齐(见【药物相互作用】)。如果无法避免合并使用中效CYP3A4抑制剂,请参阅【用法用量】的剂量调整说明。
阿伐替尼与可能延长QT间期的药物合并使用时应考虑通过ECG对QT间期进行评估。在首次即将给药之前,应进行12导联ECG检查评估,每个用药周期中医生可根据临床需要适当增加监测频率。
胃肠系统疾病
腹泻、恶心和呕吐是不可切除或转移性GIST患者最常报告的胃肠不良反应(见【不良反应】)。如发生需要治疗的胃肠不良反应,可使用止吐、止泻或抑酸药进行支持性护理。
须密切监测发生胃肠不良反应患者是否出现脱水症状,并根据标准临床实践进行治疗。
实验室检查
接受阿伐替尼治疗的不可切除或转移性GIST患者可能发生贫血、中性粒细胞减少症和血小板减少症(见【不良反应】)。接受阿伐替尼治疗期间常规应定期监测全血细胞计数。在每个新的用药周期开始前进行全血细胞计数检查,医生可根据检查结果增加监测频率。
接受阿伐替尼治疗的不可切除或转移性GIST患者可能发生胆红素与肝脏转氨酶升高(见【不良反应】)。接受阿伐替尼治疗的患者应定期监测肝功能(转氨酶、胆红素)。在每个新的用药周期开始前进行肝功能检查,医生可根据检查结果增加监测频率。
光敏性反应
阿伐替尼存在相关光毒性风险,应避免或尽量减少阳光直射。应指导患者采取措施,例如穿着防护服和涂抹高防晒系数(SPF)的防晒霜。
【价格】
在中国,阿伐替尼片有2种规格,都为每盒30片包装:
规格100mg*30片/盒,价格为¥46056元/盒
规格300mg*30片/盒,价格为¥97000元/盒
【贮藏】
密闭,不超过25℃保存。
【批准文号】
国药准字HJ20210021
【生产企业】
Catalent Nottingham
【生产地址】
8 Nottingham Business Park, orchard place, Nottingham, Nottinghamshire NG86PX UNITED KINGDOM 英国
通过以上泰吉华(阿伐替尼)说明书的介绍,相信大家对于“泰吉华(阿伐替尼)说明书”有了一定的了解。觅健小编建议大家,如出现身体不适,请及时到正规医院就诊,以免错过最佳治疗时期,从而导致病情恶化。想要了解更多泰吉华(阿伐替尼)可以继续关注觅健或者下载觅健APP!
注:以上资讯来源于网络,由觅健小编整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
热门药品